医疗器械/体外诊断试剂临床试验基本文件目录
来自:思途cro咨询 时间:2024-01-11 浏览:次
医疗器械/体外诊断试剂临床试验基本文件目录
为指导申办者和医疗器械临床试验机构开展医疗器械(含体外诊断试剂,下同)临床试验,特制定本文件目录供参考执行。
医疗器械临床试验开展顺序一般为:申办者完成临床前相关研究,选择已备案的医疗器械临床试验机构以及主要研究者,并组织临床试验方案等相关文件制定。伦理委员会审查批准该临床试验,申办者与临床试验机构签订合同后进行医疗器械临床试验项目备案;其中,对人体具有较高风险的第三类医疗器械临床试验,还应当经国务院药品监督管理部门批准。受试者签署知情同意书以及入组,研究者按照临床试验方案实施临床试验。申办者在临床试验完成后向所在地省局报告。
一、临床试验准备阶段
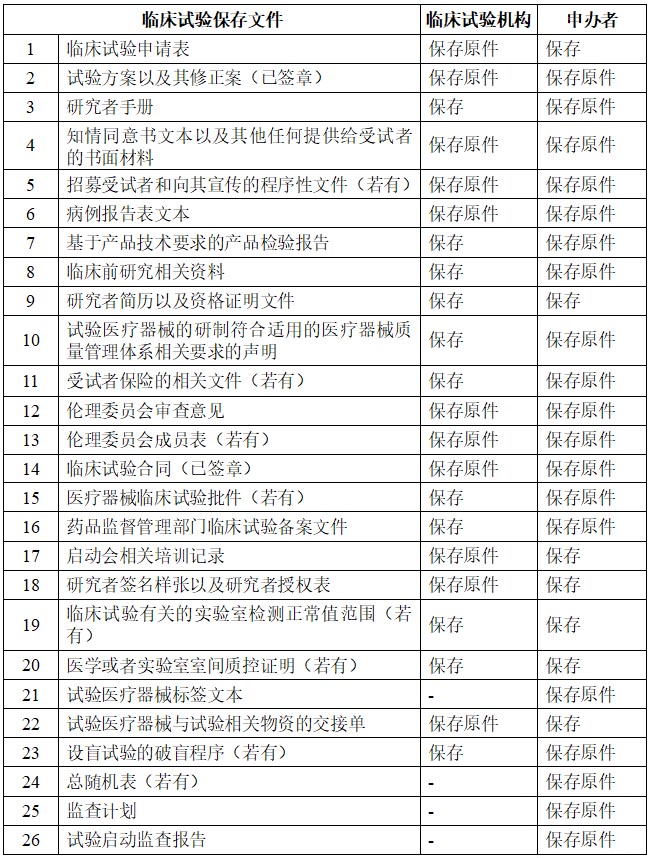
二、临床试验进行阶段
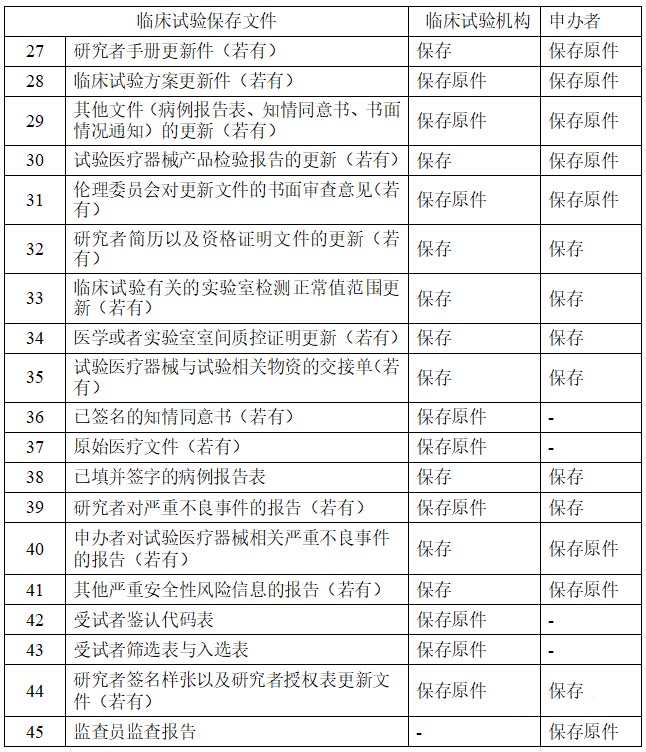
三、临床试验完成或者终止后
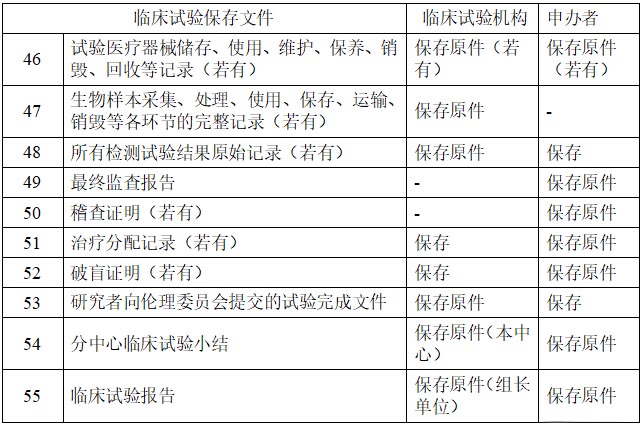
扫描下方的二维码订阅“思途CRO公众号”!聚焦中国, 放眼全球, 关注医疗器械产品合规风险,获取全球临床注册最新一手资讯。

本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。




